第67回日本神経学会学術大会 ランチョンセミナー40
アルツハイマー病の血液バイオマーカー
■座長:池内 健 先生
新潟大学脳研究所 生命科学リソース研究センター 教授
■演者:新美 芳樹 先生
東京大学医学部附属病院 認知症共生社会創成治療学 特任准教授
■日時:2026年5月22日(金)11:30~12:30
■会場:第11会場 パシフィコ横浜 会議センター 4F 418
アルツハイマー病などの神経疾患バイオマーカーをラインナップ
血液試薬
血液バイオマーカーの適正使用
- 実臨床における血液バイオマーカーは、アミロイドPET検査による脳内Aβ陽性/陰性を感度90%、特異度90%程度以上の精度で識別することが求められる[17,39]。血漿中のリン酸化タウpT217およびpT217/Aβ42は、アミロイドPET検査を参照とした時に脳内Aβ蓄積を感度90~93%、特異度91~94%、AUC (area under the curve) 0.91~0.97で検出できることが国内外から報告されており[40-42]、脳内Aβ蓄積を高い精度で検出した。そのため血漿中のリン酸化タウpT217およびpT217/Aβ42は、臨床的に活用が可能な血液バイオマーカーとして推奨される。
- Aβ42/40比などの血漿Aβ分子種比は、脳内Aβ蓄積と有意に相関することが報告されているが[43]、その精度はリン酸化タウpT217およびpT217/Aβ42よりも低いことが報告されている[44]。脳内Aβ蓄積陽性者と陰性者の血漿Aβ42/40比の変化量は比較的小さく、脳内Aβ蓄積の有無を判別する際の頑強性についての課題がある[39,45]。
- 血漿中リン酸化タウpT217およびpT217/Aβ42測定は、抗Aβ抗体薬の事前検査として行われる脳脊髄液検査やPET検査のプレスクリーニング検査として実施されることが推奨される[46]。その際には、血液バイオマーカー検査は認知症に関する十分な経験と知識を有する認知症関連学会の専門医等の医師が実施すべきであり、必要に応じて他の検査を組み合わせ、脳内Aβ蓄積のハイリスク群であるか否かについて臨床的に判断する。また検査前後に血液バイオマーカー検査に関する十分な説明を行う。
- 血液バイオマーカー検査が保険収載され、臨床現場で実施する際には、抗Aβ抗体薬および検査薬の添付文書ならびに最適使用推進ガイドラインを参照し、適切に実施する[31,32]。
- 血漿中リン酸化タウpT217およびpT217/Aβ42等の血液バイオマーカーの結果が陰性である場合、脳内Aβ蓄積を欠いている可能性が高いと判断される。しかしながら血液バイオマーカー測定結果が偽陰性を示す可能性を考慮し、担当医が臨床的にアルツハイマー病を強く疑う場合には、血液バイオマーカーの結果が陰性であっても、脳脊髄液検査やアミロイドPET検査を追加して精査することを考慮する。また、血液バイオマーカーの結果が陽性であった場合、脳脊髄液もしくはアミロイドPET検査を実施し、脳内Aβ所見が陽性であることを確認することが推奨される。脳Aβ蓄積はレビー小体型認知症等の他の認知症性疾患においても認めることがあるため、担当医は臨床所見を総合的に加味して血液バイオマーカーの結果を解釈すべきである[47-49]。
等
臨床使用の適正化:不適切な使用
以下の目的や対象者に対してバイオマーカー検査を実施することは不適切と考える。
- アルツハイマー病を含む認知症の発症前診断や発症予測を目的に無症候者を対象に行う検査
- 自覚的な物忘れ等を訴えるが、客観的には認知機能障害を認めない場合
- 認知症の重症度の判定
- 無症状のAPOE ε4保持者に対して脳内Aβ蓄積を予測する目的
- 保険収載されているアルツハイマー型認知症に対する症状改善薬(ドネペジル塩酸塩、ガランタミン臭化水素酸塩、リバスチグミン、メマンチン塩酸塩)および抗Aβ抗体薬の治療効果を判定するための使用。抗Aβ抗体薬治療により液性バイオマーカーが改善することが報告されているが[29,30]、Aβプラーク除去と液性バイオマーカー変化との相関は弱く、個々の症例において抗Aβ抗体薬の治療効果判定を液性バイオマーカーで行うことは現時点では困難である。ドナネマブ治療効果としてのAβプラーク除去の確認は、液性バイオマーカーでなくアミロイドPETを用いることが最適使用推進ガイドラインにより推奨されている[32]。
参考文献
17. Jack CR Jr, Andrews JS, Beach TG, et al. Revised criteria for diagnosis and staging of Alzheimer's disease: Alzheimer's Association Workgroup. Alzheimers Dement 20:5143-5169, 2024
29. van Dyck CH, Swanson CJ, Aisen P, et al. Lecanemab in early Alzheimer's disease. N Engl J Med 388:9-21, 2023
30. Sims JR, Zimmer JA, Evans CD, et al. Donanemab in early symptomatic Alzheimer disease: The TRAILBLAZER-ALZ 2 randomized clinical trial. JAMA 330:512-527, 2023
31. 最適使用推進ガイドライン レカネマブ(遺伝子組換え)令和5年12月 厚生労働省https://www.mhlw.go.jp/content/001180610.pdf
32. 最適使用推進ガイドライン ドナネマブ(遺伝子組換え)令和6年11月 厚生労働省 https://www.mhlw.go.jp/content/001335702.pdf
39. Schindler SE, Galasko D, Pereira AC, et al. Acceptable performance of blood biomarker tests of amyloid pathology - recommendations from the Global CEO Initiative on Alzheimer‘s Disease. Nat Rev Neurol 20:426-439, 2024
40. Palmqvist S, Tideman P, Mattsson-Carlgren N, et al. Blood biomarkers to detect Alzheimer disease in primary care and secondary care. JAMA 332:1245-1257, 2024
41. Niimi Y, Janelidze S, Sato K, et al. Combining plasma Aβ and p-tau217 improves detection of brain amyloid in non-demented elderly. Alzheimers Res Ther 16:115, 2024
42. Barthélemy NR, Salvadó G, Schindler SE, et al. Highly accurate blood test for Alzheimer's disease is similar or superior to clinical cerebrospinal fluid tests. Nat Med 30:1085-1095, 2024
43. Brand AL, Lawler PE, Bollinger JG, et al. The performance of plasma amyloid beta measurements in identifying amyloid plaques in Alzheimer's disease: a literature review. Alzheimers Res Ther 14:195, 2022
44. Schindler SE, Petersen KK, Saef B, et al. Head-to-head comparison of leading blood tests for Alzheimer's disease pathology. Alzheimers Dement. 20:8074-8096, 2024
45. Rabe C, Bittner T, Jethwa A, et al. Clinical performance and robustness evaluation of plasma amyloid-β42/40 prescreening. Alzheimers Dement 19:1393-1402, 2023
46. Mattsson-Carlgren N, Collij LE, Stomrud E, et al. Plasma biomarker strategy for selecting patients with Alzheimer disease for antiamyloid immunotherapies. JAMA Neurol 81:69-78, 2024
47. Hansson O, Edelmayer RM, Boxer AL, et al. The Alzheimer's Association appropriate use recommendations for blood biomarkers in Alzheimer's disease. Alzheimers Dement 18:2669-2686, 2022.
48. Mielke MM, Anderson M, Ashford JW, et al. Considerations for widespread implementation of blood-based biomarkers of Alzheimer's disease. Alzheimers Dement 20:8209-8215, 2024
49. Mielke MM, Anderson M, Ashford JW, et al. Recommendations for clinical implementation of blood-based biomarkers for Alzheimer's disease. Alzheimers Dement 20:8216-8224, 神医学会監修.
(令和6年度厚生労働科学研究費補助金 [厚生労働科学特別研究事業/研究代表者:冨本秀和] にて作成)
※国内では現時点で体外診断用医薬品未承認のため、臨床診断等には使用できません。
リン酸化タウ217(血漿)測定キット(IC)
※本製品は認定検査試薬であり診断目的に使用することはできません。

Sebastian P et al.
Plasma phospho-tau217 for Alzheimer’s disease
diagnosis in primary and secondary care using a fully
automated platform | Nature Medicine
*外部サイトに遷移します
- 掲載雑誌:nature medicine
- タイトル:Plasma phospho-tau217 for Alzheimer's disease diagnosis in primary and secondary care using a fully automated platform
- 掲載日 :2025年4月9日
- 関連製品:※Lumipulse G pTau 217(RUO)
本文献のポイント
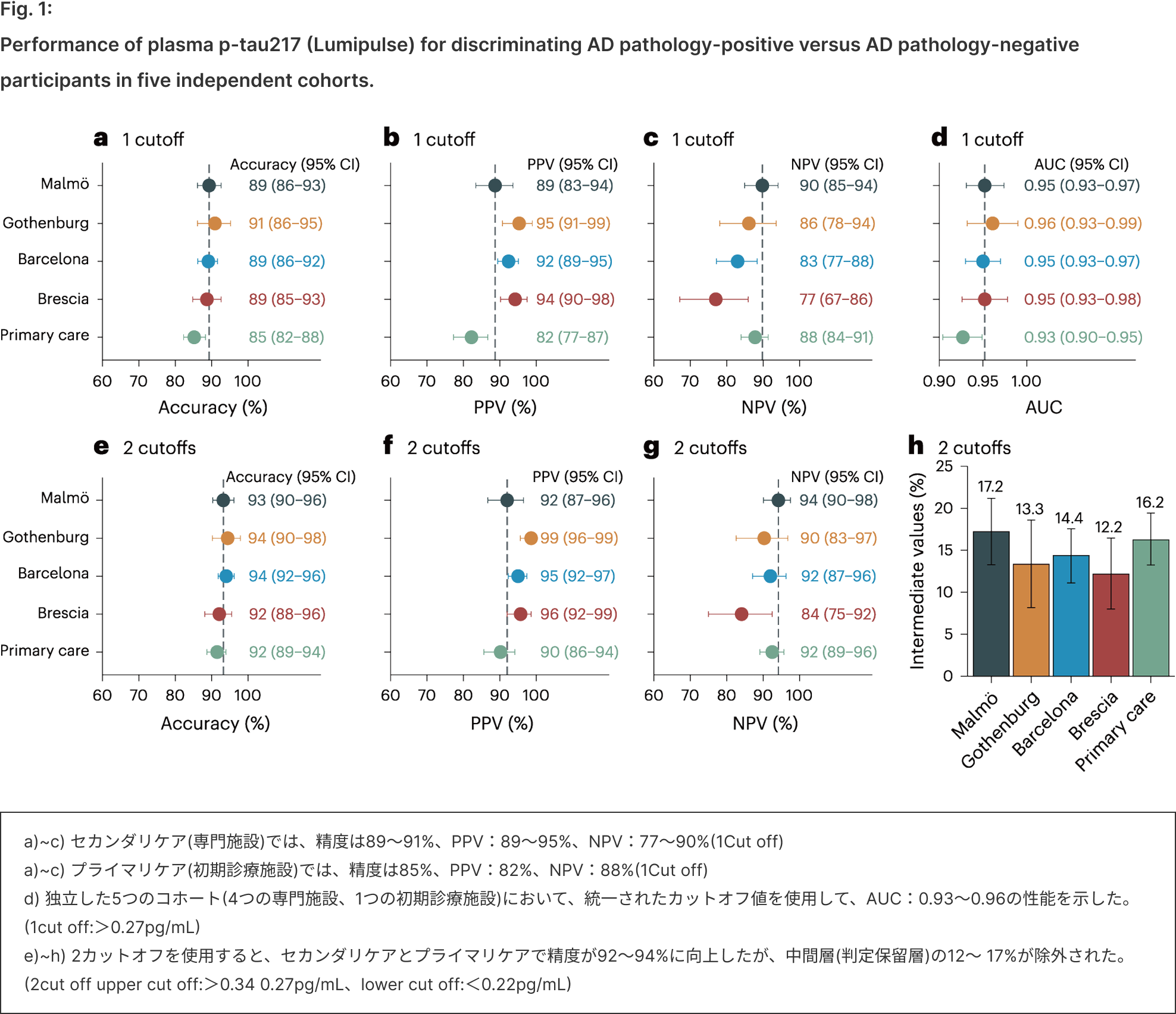
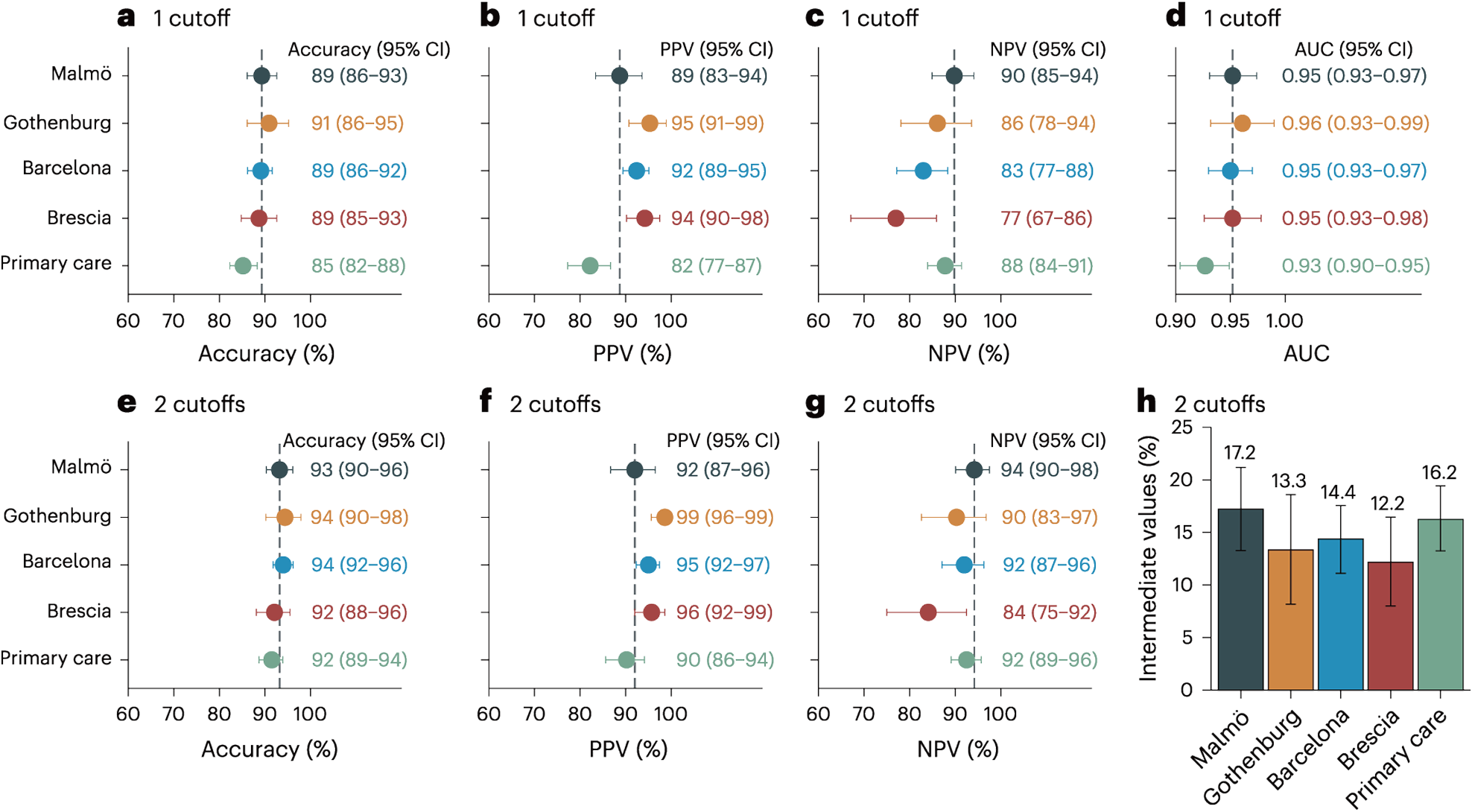
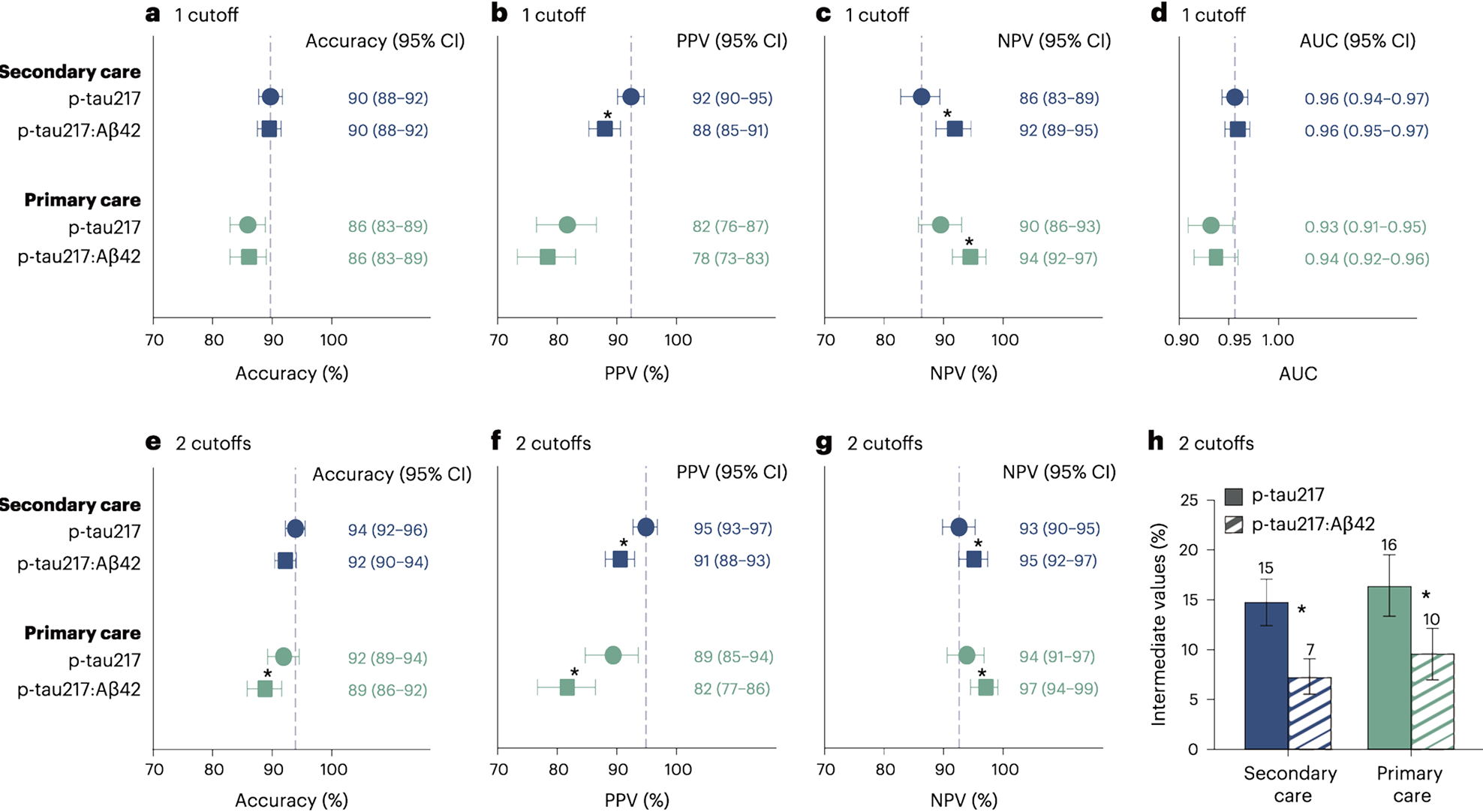
- 独立した5つのコホート(4つの専門施設、1つの初期診療施設)において、統一されたカットオフ値を使用して、AUC:0.93~0.96の性能を示した (1cut off:>0.27pg/mL)
- セカンダリケア(専門施設)では、精度は89〜91%、PPV:89〜95%、NPV:77〜90%(1Cut off)
- プライマリケア(初期診療施設)では、精度は85%、PPV:82%、NPV:88%(1Cut off)
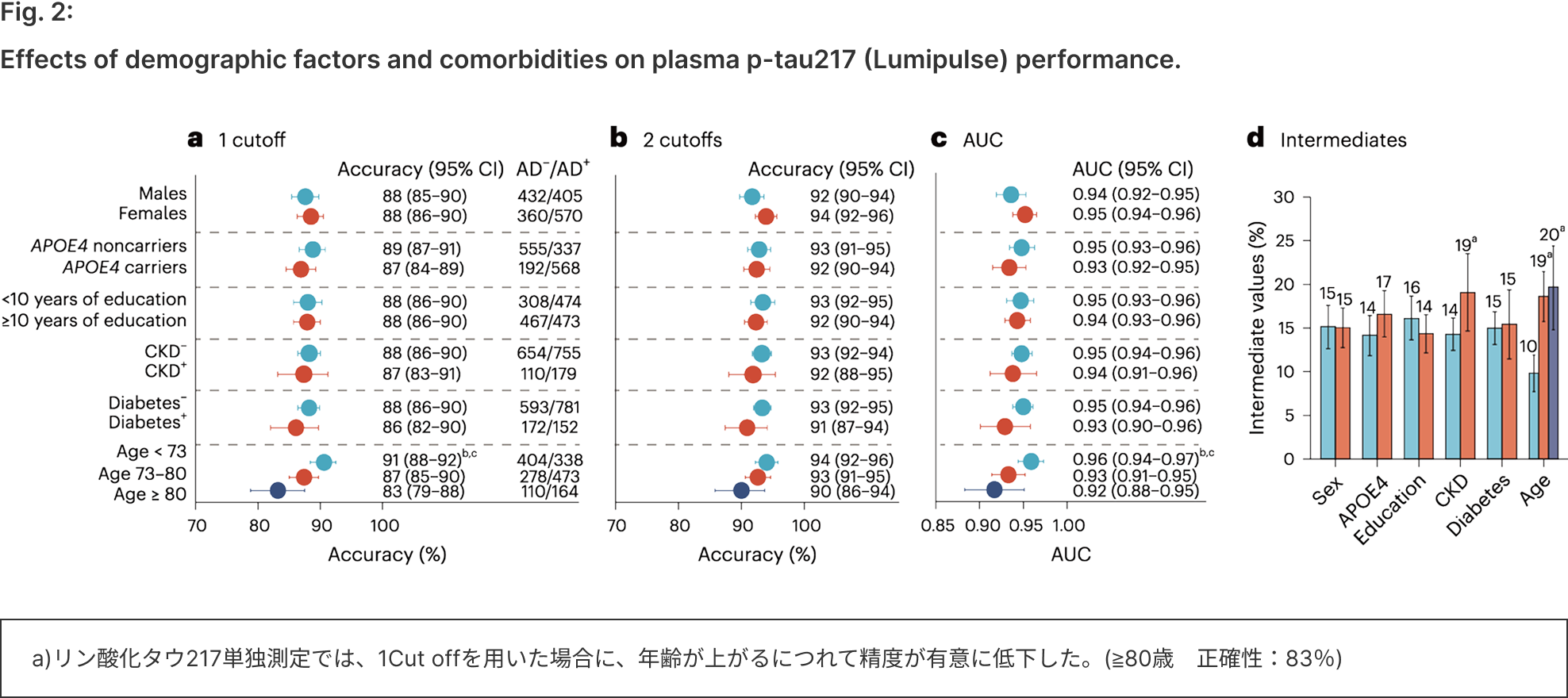
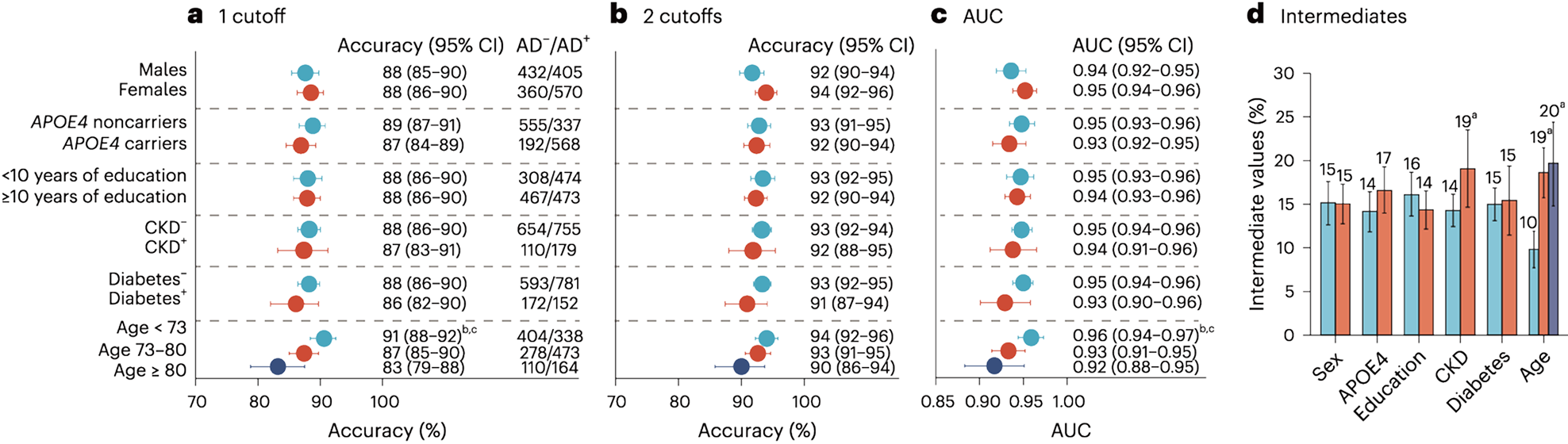
- 80≥歳の参加者では精度が低下する傾向がみられた(83%)(1Cut off)
- 慢性腎臓病、糖尿病、性別、APOE遺伝子型、認知機能レベルの影響を受けなかった(慢性腎臓病の影響については、p-tau217単独では、有意差がみられた)
- 2カットオフを使用すると、セカンダリケアとプライマリケアで精度が92〜94%に向上したが、中間層(判定保留層)の12〜17%が除外された。(2cut off upper cut off:>0.34 0.27pg/mL、lower cut off:<0.22pg/mL)
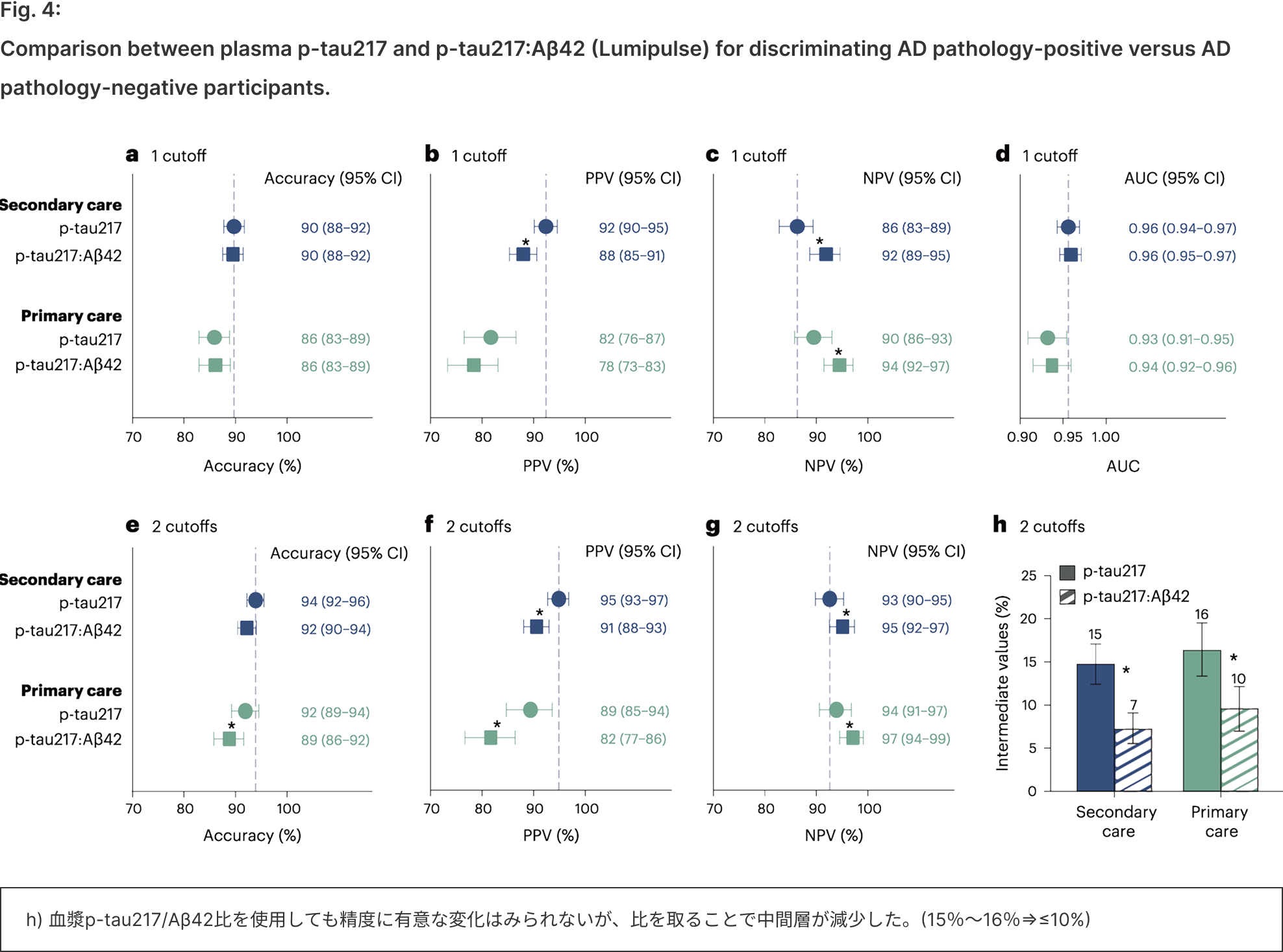
- 血漿p-tau217/Aβ42比を使用しても精度は変わらないが、中間層が減少した。(≤10%)
結論
血漿p-tau217を測定するための全自動アッセイ(Lumipulse)は、事前に確立されたカットオフを使用し、さまざまな専門施設および初期診療施設におけるAD病理の検出において高い精度を示した。これらの有望な知見は、本技術を様々な環境で追加検証することで、正確なAD診断のための日常的な臨床診療に血液バイオマーカー(BBM)の採用を促進する可能性がある。






脳脊髄液(CSF)試薬
ルミパルス® β-アミロイド1-42
● 使用目的
脳脊髄液中のβ-アミロイド1-42の測定(脳内アミロイドβの蓄積状態把握の補助)
● 判定法
測定結果の判定は、 β-アミロイド1-42濃度と、β-アミロイド1-40濃度から算出された β-アミロイド1-42/1-40比で行う
● 重要な基本的注意
認知症の診断に関連する十分な知識及び経験を有する医師が、検査の原理及び結果の 解釈を十分に理解した上で、関連学会等の適正使用指針に従って使用すること
ルミパルス® β-アミロイド1-40
● 使用目的
脳脊髄液中のβ-アミロイド1-40の測定(脳内アミロイドβの蓄積状態把握の補助)
ルミパルス® リン酸化タウ181
● 使用目的
脳脊髄液中の181位リン酸化タウ蛋白の測定(アルツハイマー型認知症及び軽度認知機能障害(MCI)に限る)
ルミパルス® 総タウ
● 使用目的
ヒト脳脊髄液中のタウ蛋白の測定(クロイツフェルト・ヤコブ病及びアルツハイマー型認知症の診断補助)
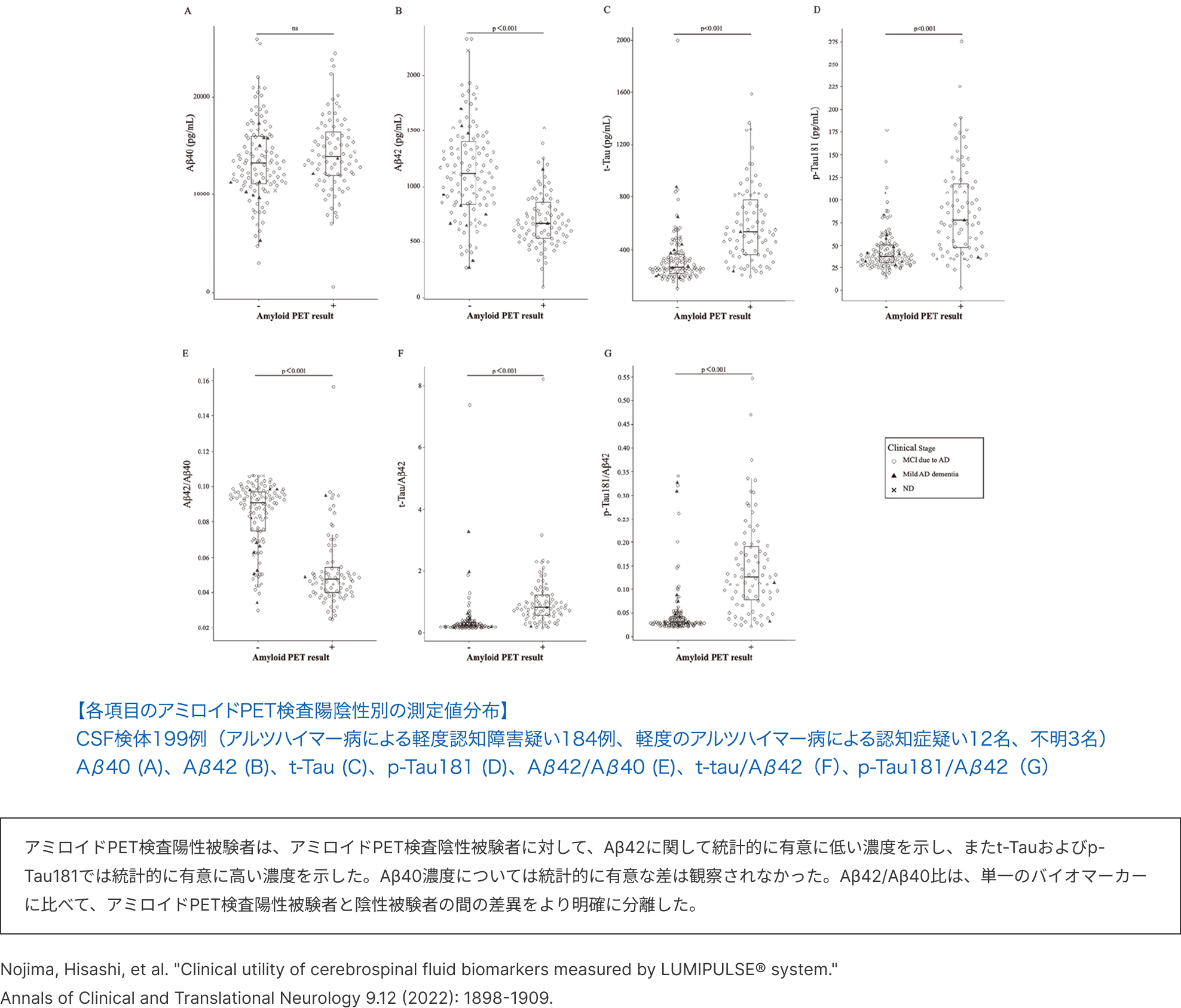
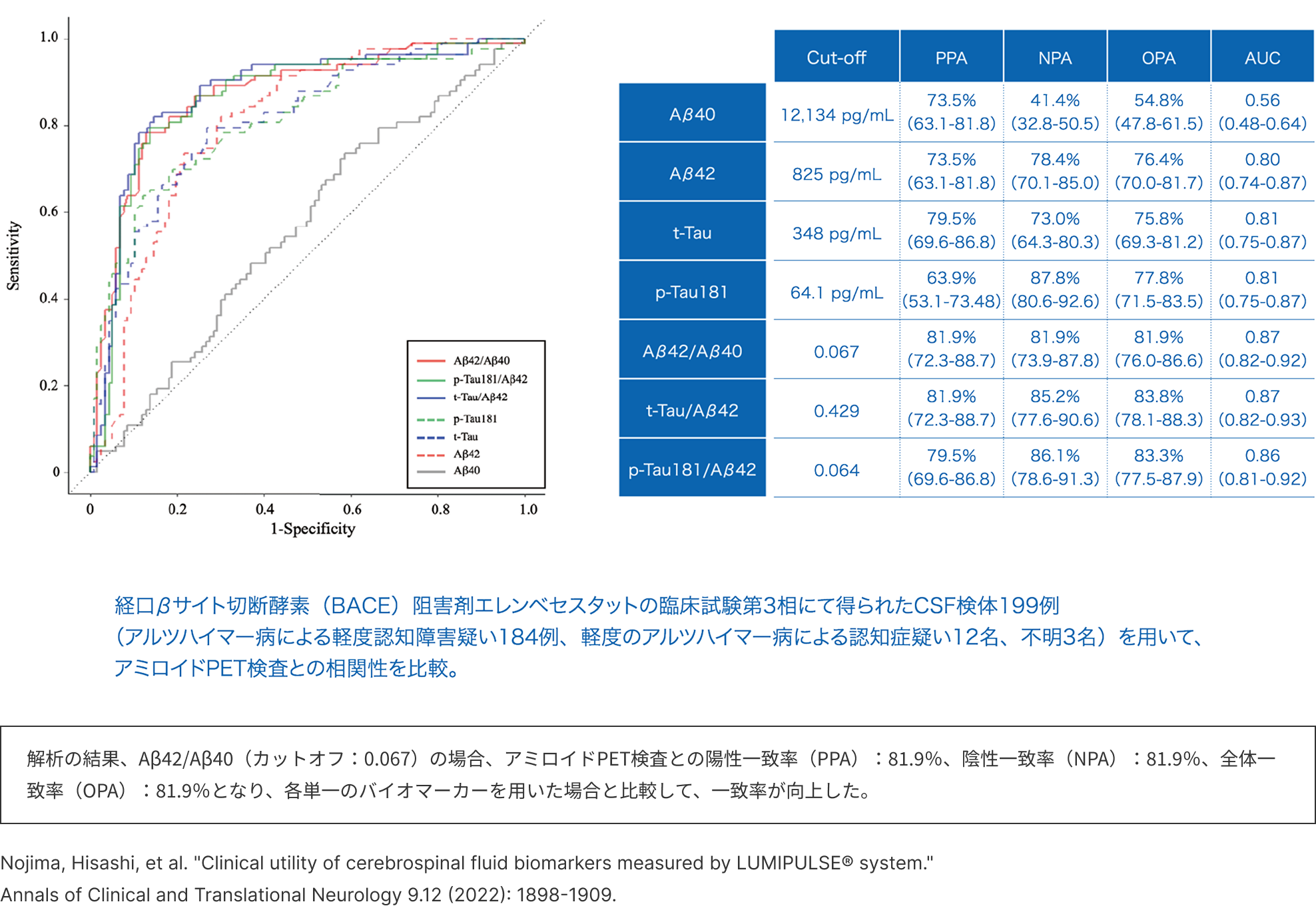
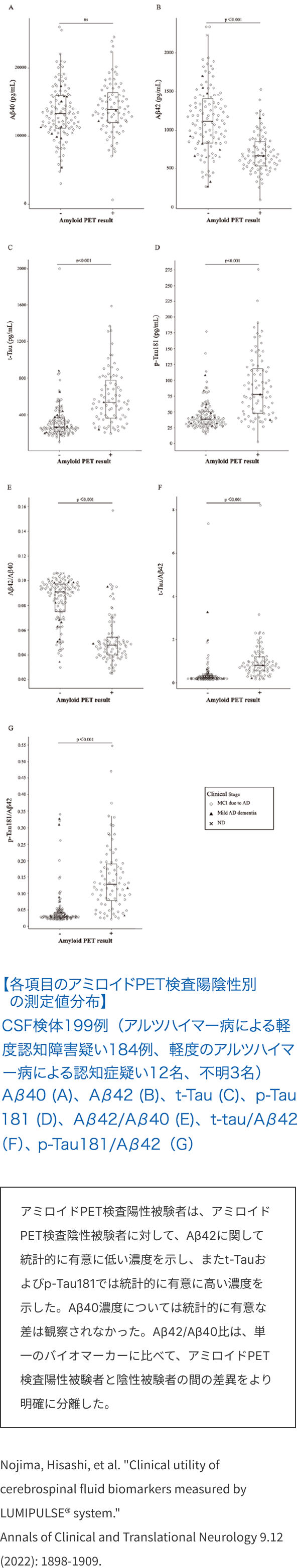
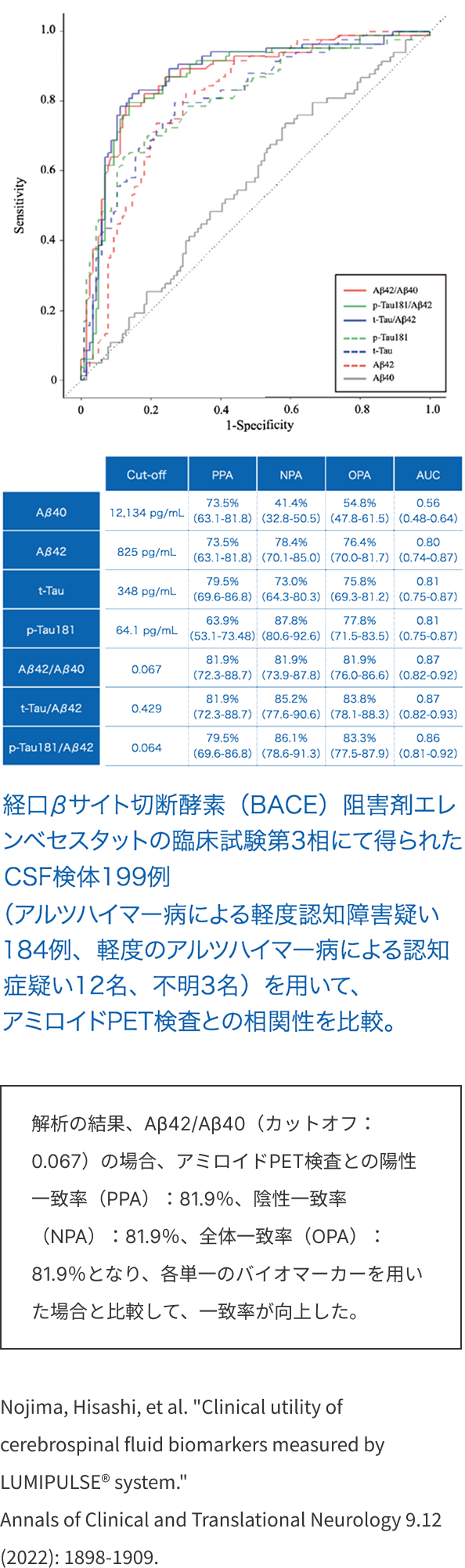
アミロイド β42/40比
● 体外診断用医薬品の使用目的としての対象疾患
脳内アミロイドβの蓄積状態把握の補助(疾患名の記載なし)
● 保険収載上の対象疾患と算定方法
効能又は効果としてアルツハイマー病による軽度認知障害及び軽度の認知症の進行抑制を有する医薬品に係る厚生労働省の定める最適使用推進ガイドラインに沿って、アルツハイマー病による軽度認知障害又は軽度の認知症が疑われる患者等に対し、効能又は効果としてアルツハイマー病による軽度認知障害及び軽度の認知症の進行抑制を有する医薬品の投与の要否を判断する目的でアミロイドβ病理を示唆する所見を確認するため、CLEIA法により、脳脊髄液中のβ‒アミロイド1‒42及びβ‒アミロイド1‒40を同時に測定した場合、患者1人につき1回に限り算定する。ただし、効能又は効果としてアルツハイマー病による軽度認知障害及び軽度の認知症の進行抑制を有する医薬品の投与中止後に初回投与から18か月を超えて再開する場合は、さらに1回に限り算定できる。
● 保険点数
1282点
タウ蛋白
● 体外診断用医薬品の使用目的としての対象疾患
クロイツフェルト・ヤコブ病及びアルツハイマー型認知症の診断補助に用いる
● 保険収載上の対象疾患と算定方法
タウ蛋白(髄液)は、クロイツフェルト・ヤコブ病の診断を目的に、1患者につき1回に限り算定する
● 保険点数
622点(※CJDのみ)
リン酸化タウ蛋白
● 体外診断用医薬品の使用目的としての対象疾患
アルツハイマー型認知症及び軽度認知機能障害(MCI)に限る
● 保険収載上の対象疾患と算定方法
リン酸化タウ蛋白(髄液)は、認知症の診断を目的に、1患者につき1回に限り算定する
● 保険点数
641点
アミロイドβ42/40比(髄液)に関する留意事項
- 抗体医薬品(レカネマブ、ドナネマブ)の最適使用推進ガイドラインに沿って、抗体医薬品の投与の要否を判断する目的に対して1人1回限り算定。
- 抗体医薬品の投与中止後に初回投与から18か月を超えて再開する場合は、さらに1回限り算定できる。
- リン酸化タウ蛋白(髄液)と同時測定の場合は主たるもののみを算定。
令和6年度診療報酬改定
・「診療報酬の算定方法の一部改正に伴う実施上の留意事項について」
(令和6年3月5日保医発0305第4号)の一部改正について
ルミパルス® β−アミロイド1-40
ルミパルス® β−アミロイド1-42

日本初
β-アミロイド1-42(脳脊髄液)およびβ-アミロイド1-40(脳脊髄液)の2項目は体外診断用医薬品として日本で初の承認品。

測定精度
・ルミパルスシステムによる全自動測定に対応
・アミロイドPET検査との高い判定一致率(βアミロイド1-42/1-40比)

抗体医薬品(レカネマブ ※1、ドナネマブ※2)の投薬前検査
"効能又は効果としてアルツハイマー病による軽度認知障害及び軽度の認知症の進行抑制を有する医薬品"の投薬前検査に使用可能
※1
製造販売元(輸入):エーザイ株式会社、販売提携:バイオジェン・ジャパン株式会社
※2 製造販売元:日本イーライリリー株式会社
β-アミロイド1-42について、測定システムが異なる富士レビオ製品(海外含む)の3試薬を用いて再現性を比較
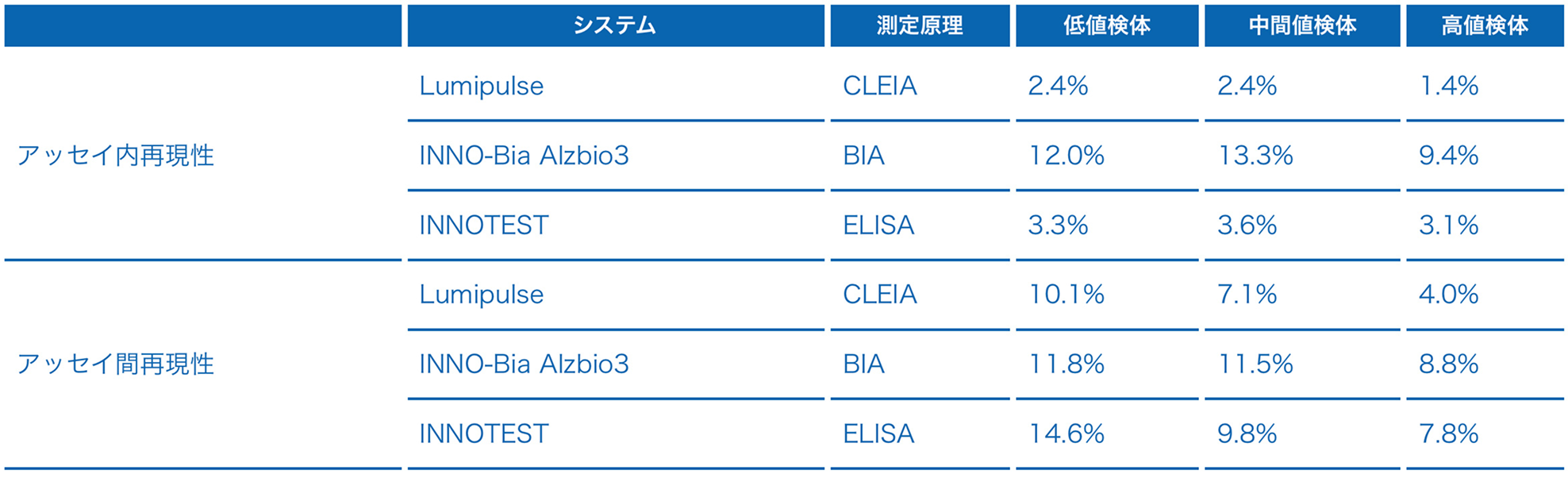
ルミパルスはアッセイ内、アッセイ間再現性ともに良好
Kollhoff, Alexander L., Jennifer C. Howell, and William T.
Hu. “Automation vs. experience: Measuring Alzheimerʼs
beta-amyloid 1–42 peptide in the CSF. ”
Frontiers in aging neuroscience 10 (2018): 253.より引用作表
ルミパルス® G1200
ルミパルス® G600Ⅱ用試薬
製品パンフレットをクリックすると、H.U.フロンティアのページに遷移します。(閲覧にはLabsync®会員への登録が必要です)
CODE No. 231524
ルミパルス β−アミロイド1-40
免疫反応カートリッジ
免疫反応カートリッジ
CODE No. 260241
ルミパルス β−アミロイド1-40
β−アミロイド1-40キャリブレータセット
β−アミロイド1-40キャリブレータセット
CODE No. 260265
LPコントロール・β−アミロイド
CODE No. 230336
ルミパルス β−アミロイド1-42
免疫反応カートリッジ
免疫反応カートリッジ
CODE No. 260258
ルミパルス β−アミロイド1-42
β−アミロイド1-42キャリブレータセット
β−アミロイド1-42キャリブレータセット
CODE No. 260265
LPコントロール・β−アミロイド
CODE No. 230350
ルミパルス リン酸化タウ181
免疫反応カートリッジ
免疫反応カートリッジ
CODE No. 260227
ルミパルス リン酸化タウ181
標準リン酸化タウ181溶液
標準リン酸化タウ181溶液
CODE No. 260234
LPコントロール・リン酸化タウ181
CODE No. 230312
ルミパルス 総タウ
免疫反応カートリッジ
免疫反応カートリッジ
CODE No. 260203
ルミパルス 総タウ
総タウキャリブレータセット
総タウキャリブレータセット






